Опыт1 Получение и свойства метана
В пробирку поместите выданную учителем смесь безводного ацетата натрия и натронной извести 1:2. Про-бирку закройте пробкой с газоотводной трубкой и за-крепите наклонно вверх в лапке штатива. Содержимое пробирки нагрейте в пламени спиртовки. Напишите уравнение протекающей реакции.Выделяющийся газ пропустите через подкисленный раствор перманганата калия и бромную воду (если она отсутствует, то можно воспользоваться аналогом— иодной водой, которую готовят, приливая 2—3капли спиртовой настойки иода к 1—2мл воды). Что наблюдаете?Выделяющийся газ подожгите. Обратите внимание на характер горения. Напишите уравнение реакции горения метана.
Вопросы
1. Почему не наблюдается изменения окраски раствора перманганата калия и бромной воды при пропускании через них метана?
2. О чём свидетельствует характер пламени метана?
Получение метана(видео)
Отношение метана к перманганату калия и бромной воде(видео)
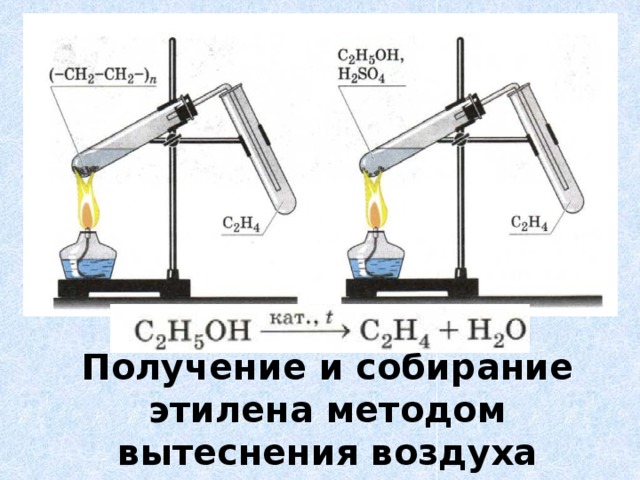
Опыт 2.Получение и свойства этилена (этена)
В пробирку с газоотводной трубкой поместите концентрированную серную кислоту и этиловый спирт в соотношении 3/1.Укрепите пробирку в лапке штатива горизонтально с небольшим наклоном . Содержимое нагрейте на пламени спиртовки. Напишите уравнение реакции получения этилена.Выделяющийся этилен про-пустите через подкисленный раствор перманганата калия и бромную (иодную) воду. Что наблюдаете? Напишите уравнения протекающих реакций.Переверните пробку в пробирке газоотводной трубкой вверх (осторожно, горячая пробирка!) и подожгите выделяю-щийся этилен. Обратите внимание на характер пламени этилена, сравните его с пламенем метана. Напишите уравнение реакции горения этилена.
Вопросы:
1. Чем обусловлен различный характер горения метана и этилена?
2. Какими способами получают этилен в лаборатории и в промышленности? Напишите уравнения реакций.
3. Почему этилен обесцвечивает растворы бромной воды и перманганата калия?
Получение этилена(Видеофрагмент)
Опыт 3.Получение и свойства ацетилена
В сухой прибор для получения газов поместите 2 кусочка карбида кальция, завёрнутые в фильтровальную бумагу. С помощью пипетки добавьте в пробирку несколько капель насыщенного раствора хлорида натрия (с водой реакция протекает слишком бурно). Закройте прибор пробкой с газоотводной трубкой. Напишите уравнение реакции карбида кальция с водой.Выделяющийся газ пропустите через подкисленный раствор перманганата калия и бромную воду. Что наблюдаете?Подожгите газ у конца газоотводной трубочки. Отметьте характер горения ацетилена.По окончании опыта, после того как перестал выделяться ацетилен, выньте из пробирки пробку с газоотводной трубкой и добавьте в пробирку каплю раствора фенолфталеина. Что наблюдаете?
Вопросы:
1. Зачем кусочки карбида кальция заворачивают в фильтровальную бумагу?
2. Почему ацетилен обесцвечивает бромную воду и раствор перманганата калия?
3. Почему ацетилен горит коптящим пламенем?
4. Почему фенолфталеин изменяет окраску при добавлении к продуктам реакции гидролиза карбида кальция?
Получение ацетилена(видео)
Горение ацетилена (видео)
Оформление работы
Комментариев нет:
Отправить комментарий